Los colores que presentan los vegetales son debidos a unos compuestos químicos llamados pigmentos. El color que presenta un determinado órgano vegetal depende generalmente del predominio de uno u otro pigmento o la combinación de ellos. Además, algunos de los pigmentos que condicionan el color están estrechamente ligados a las actividades fisiológicas del propio vegetal. Los pigmentos vegetales se clasifican en tres categorías principales que van a ser estudiados en esta práctica:
de ellos. Además, algunos de los pigmentos que condicionan el color están estrechamente ligados a las actividades fisiológicas del propio vegetal. Los pigmentos vegetales se clasifican en tres categorías principales que van a ser estudiados en esta práctica:
oCarotenos. de ellos. Además, algunos de los pigmentos que condicionan el color están estrechamente ligados a las actividades fisiológicas del propio vegetal. Los pigmentos vegetales se clasifican en tres categorías principales que van a ser estudiados en esta práctica:
de ellos. Además, algunos de los pigmentos que condicionan el color están estrechamente ligados a las actividades fisiológicas del propio vegetal. Los pigmentos vegetales se clasifican en tres categorías principales que van a ser estudiados en esta práctica:o Clorofilas.
o Flavonoides.
1.1. CAROTENOS.
Son pigmentos amarillos, naranjas o rojos. Estos siempre acompañan a la clorofila en una relación de tres a cuatro partes de clorofila por una de carotenoides. Son insolubles en agua y solubles en grasas y disolventes orgánicos. Existen varios tipos de carotenoides, que difieren en cuanto a solubilidad:
o Carotenos: hidrocarburos solubles en éter de petróleo.
o Xantofilas: derivados oxigenados de los carotenos y solubles en alcohol.
Como ejemplos de carotenoides, tenemos:
o Carotenos: hidrocarburos solubles en éter de petróleo.
o Xantofilas: derivados oxigenados de los carotenos y solubles en alcohol.
Como ejemplos de carotenoides, tenemos:

Se encuentra presente en zanahoria y la mayoría de plantas verdes.
Licopeno:

Está presente en numerosas plantas como el tomate.
Una característica de estas moléculas es que cuanto menor es el número de enlaces dobles conjugados, más se incrementa el color amarillo. Por tanto, el -caroteno es menos naranja que el caroteno.
En estas moléculas, el efecto de la temperatura o de pH es pequeño, como más adelante veremos. Pero sí son susceptibles a la oxidación y pérdida de color por este motivo. Para evitarlo, podemos tratarlos con sulfuroso de las frutas.
1.2. CLOROFILAS.
Son los pigmentos verdes de las plantas que se encuentran especialmente en la hoja. Son los encargados de captar la energía de la luz para sus funciones vitales.
Son pigmentos http://ilovepedospe.blogspot.com/ insolubles en agua, pero sí en grasas y disolventes como el éter.
Podemos distinguir entre estos:
o Clorofila a: es de olor azul-verdoso.
o Clorofila b: de color amarillo-verdoso.
Dicho color se ve afectado por la temperatura, sufriendo una intensificación. El pH también influye sobre estas macromoléculas:

Las clorofilas son sensibles a los ácidos. En un medio ácido, son capaces de sustituir el átomo de magnesio por dos de hidrógeno, dando lugar a las feofitinas. En este paso, se produce una marcada alteración del color de los alimentos. Iones de cobre y zinc, pueden unirse a dicha molécula, para restituir el color verde inicial de la planta. Bien es cierto que no es recomendable para alimentos, destinados http://ilovepedospe.blogspot.com/ al consumo. También la temperatura puede afectar la conversión de clorofila en feofitina.
1.3. FLAVONOIDES.
Son pigmentos muy distribuidos a lo largo de las plantas. Entre ellos se encuentran las antocianinas y las antoxantinas.
1.3.3. Antocianinas.
Son pigmentos rojos, púrpuras o azules responsables del brillo de las pieles rojas de patatas, rábanos,…

Su color varía con la estructura molecular, si aumenta la hidroxilación, aumenta la coloración azulada.
Estas moléculas son deficientes en electrones y muy reactivas. Tanto, que pueden experimentar cambios durante el procesamiento y posterior almacenamiento. El color varía con el pH.
En medio ácido, es un http://ilovepedospe.blogspot.com/ catión de color rijo. Cuanto más bajo sea el pH, más intenso será el color. A pH neutro, no tiene carga y es de color violeta. En medio ácido, es azul. En cuanto al color, si aumentamos la temperatura, se pueden dar cambios irreversibles en su estructura, que causan el deterioro del color.
1.3.4. Antoxantinas.
Son pigmentos casi incoloros o amarillo pálido solubles en agua y presentes en hortalizas débilmente coloreadas.
En medio ácido, son blancos mientras que en medio básico presentan una coloración amarilla. En cuanto a la presencia de metales, dichos pigmentos tienen la capacidad de quelarlos, lo que puede dar lugar a su decoloración o la aparición de una coloración en tonos marrones. Así por ejemplo, este componente lo http://ilovepedospe.blogspot.com/ podemos encontrar en la patata, la cual al reaccionar con los utensilios de cocina metálicos adquiere una tonalidad marrón. No obstante este efecto con metales no se estudiará en la práctica y por ello no comentamos con más detalle este fenómeno.
1.3.5. Leucoantocianinas.
Compuestos flavonoides que dan color a algunos alimentos enlatados, y que están formados por compuestos fenólicos coloreados.
Industrialmente, es interesante conocer como se comportan los citados pigmentos contenidos en las frutas y en las verduras frente a cambios de pH y de temperatura, ya que en el procesado de estos productos, muchas veces se requiere un tratamiento térmico o un escaldado previo a su conservación, lo http://ilovepedospe.blogspot.com/ cual podría producir la decoloración del alimento y en tal caso, sería necesario emplear uncolorante para satisfacer los criterios de calidad referidos al color: los consumidores prefieren productos con un color bonito y apetecible antes que un producto incoloro.
Por ello, en la práctica analizaremos estos aspectos en algunos de los pigmentos antes comentados, cada uno de los cuales estará contenido en una verdura diferente tal y como a continuación explicaremos. Así trabajaremos con la espinaca, la chirivía, la lombarda y la zanahoria.
ELABORACIÓN
Como hemos dicho, en esta práctica extraeremos los pigmentos de los vegetales mencionados para analizarlos y http://ilovepedospe.blogspot.com/ comprobar el efecto del pH y temperatura sobre ellos.
Para ello, llevaremos a cabo los siguientes pasos:
1) Pesar 50 gramos de hortaliza y licuarla (en nuestro caso la chirivía).
2) Recoger dicha cantidad en un vaso que contenga 40 ml de:
o Acetona; si son espinacas o zanahorias.
o Agua; si son lombardas o chirivía.
3) Homogeneizar la muestra durante unos dos minutos.
4) Filtrar al vacío y conservar el líquido filtrado a analizar.
A continuación, los pasos siguientes se levarán a cabo para todos los pigmentos sintetizados (tanto la chirivía, como las hortalizas del resto de nuestros compañeros)
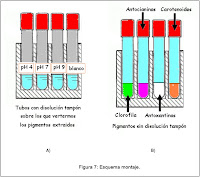
5) Para cada pigmento, preparar 4 tubos de pH distinto (blanco, 4,7 y 9).
6) Introducir en cada tubo 2 ml de los pigmentos a analizar.
7) En uno de los tubos de cada pigmento, verter gota a gota la disolución tampón de pH 4, hasta observar color.
8) Introducir el mismo número de gotas de las otras disoluciones tampón y el agua en el resto de los tubos del mismo pigmento.
9) Anotar los cambios observados.
10) Colocar los tubos en un baño se agua hirviendo durante unos 5 minutos.
11) Anotar de nuevo los cambios.
BIBLIOGRAFÍA
o Manual de Química y Bioquímica de los Alimentos. T.P. Coultate. Editorial Acribia S.A. 2ª Edición. 1998.
o http://www.monografias.com/trabajos13/cloro/cloro.shtml
o http://www.food-info.net/es/caro/stru.htm
o http://www.ghmgroup.com/interior.php?IDN=9
o http://otda.state.ny.us/main/language/spanish/FSNEP/2006-09-Shop-SP.pdf
o http://www.saludymedicinas.com.mx/nota.asp?id=2046
o http://www.adaptogeno.com/svms/noticias/noticia311.asp
o http://catarina.udlap.mx/u_dl_a/tales/documentos/lia/acevedo_c_ar/capitulo4.pdf
Una característica de estas moléculas es que cuanto menor es el número de enlaces dobles conjugados, más se incrementa el color amarillo. Por tanto, el -caroteno es menos naranja que el caroteno.
En estas moléculas, el efecto de la temperatura o de pH es pequeño, como más adelante veremos. Pero sí son susceptibles a la oxidación y pérdida de color por este motivo. Para evitarlo, podemos tratarlos con sulfuroso de las frutas.
1.2. CLOROFILAS.
Son los pigmentos verdes de las plantas que se encuentran especialmente en la hoja. Son los encargados de captar la energía de la luz para sus funciones vitales.
Son pigmentos http://ilovepedospe.blogspot.com/ insolubles en agua, pero sí en grasas y disolventes como el éter.
Podemos distinguir entre estos:
o Clorofila a: es de olor azul-verdoso.
o Clorofila b: de color amarillo-verdoso.
Dicho color se ve afectado por la temperatura, sufriendo una intensificación. El pH también influye sobre estas macromoléculas:

Las clorofilas son sensibles a los ácidos. En un medio ácido, son capaces de sustituir el átomo de magnesio por dos de hidrógeno, dando lugar a las feofitinas. En este paso, se produce una marcada alteración del color de los alimentos. Iones de cobre y zinc, pueden unirse a dicha molécula, para restituir el color verde inicial de la planta. Bien es cierto que no es recomendable para alimentos, destinados http://ilovepedospe.blogspot.com/ al consumo. También la temperatura puede afectar la conversión de clorofila en feofitina.
1.3. FLAVONOIDES.
Son pigmentos muy distribuidos a lo largo de las plantas. Entre ellos se encuentran las antocianinas y las antoxantinas.
1.3.3. Antocianinas.
Son pigmentos rojos, púrpuras o azules responsables del brillo de las pieles rojas de patatas, rábanos,…

Su color varía con la estructura molecular, si aumenta la hidroxilación, aumenta la coloración azulada.
Estas moléculas son deficientes en electrones y muy reactivas. Tanto, que pueden experimentar cambios durante el procesamiento y posterior almacenamiento. El color varía con el pH.
En medio ácido, es un http://ilovepedospe.blogspot.com/ catión de color rijo. Cuanto más bajo sea el pH, más intenso será el color. A pH neutro, no tiene carga y es de color violeta. En medio ácido, es azul. En cuanto al color, si aumentamos la temperatura, se pueden dar cambios irreversibles en su estructura, que causan el deterioro del color.
1.3.4. Antoxantinas.
Son pigmentos casi incoloros o amarillo pálido solubles en agua y presentes en hortalizas débilmente coloreadas.
En medio ácido, son blancos mientras que en medio básico presentan una coloración amarilla. En cuanto a la presencia de metales, dichos pigmentos tienen la capacidad de quelarlos, lo que puede dar lugar a su decoloración o la aparición de una coloración en tonos marrones. Así por ejemplo, este componente lo http://ilovepedospe.blogspot.com/ podemos encontrar en la patata, la cual al reaccionar con los utensilios de cocina metálicos adquiere una tonalidad marrón. No obstante este efecto con metales no se estudiará en la práctica y por ello no comentamos con más detalle este fenómeno.
1.3.5. Leucoantocianinas.
Compuestos flavonoides que dan color a algunos alimentos enlatados, y que están formados por compuestos fenólicos coloreados.
Industrialmente, es interesante conocer como se comportan los citados pigmentos contenidos en las frutas y en las verduras frente a cambios de pH y de temperatura, ya que en el procesado de estos productos, muchas veces se requiere un tratamiento térmico o un escaldado previo a su conservación, lo http://ilovepedospe.blogspot.com/ cual podría producir la decoloración del alimento y en tal caso, sería necesario emplear uncolorante para satisfacer los criterios de calidad referidos al color: los consumidores prefieren productos con un color bonito y apetecible antes que un producto incoloro.
Por ello, en la práctica analizaremos estos aspectos en algunos de los pigmentos antes comentados, cada uno de los cuales estará contenido en una verdura diferente tal y como a continuación explicaremos. Así trabajaremos con la espinaca, la chirivía, la lombarda y la zanahoria.
ELABORACIÓN
Como hemos dicho, en esta práctica extraeremos los pigmentos de los vegetales mencionados para analizarlos y http://ilovepedospe.blogspot.com/ comprobar el efecto del pH y temperatura sobre ellos.
Para ello, llevaremos a cabo los siguientes pasos:
1) Pesar 50 gramos de hortaliza y licuarla (en nuestro caso la chirivía).
2) Recoger dicha cantidad en un vaso que contenga 40 ml de:
o Acetona; si son espinacas o zanahorias.
o Agua; si son lombardas o chirivía.
3) Homogeneizar la muestra durante unos dos minutos.
4) Filtrar al vacío y conservar el líquido filtrado a analizar.
A continuación, los pasos siguientes se levarán a cabo para todos los pigmentos sintetizados (tanto la chirivía, como las hortalizas del resto de nuestros compañeros)
5) Para cada pigmento, preparar 4 tubos de pH distinto (blanco, 4,7 y 9).
6) Introducir en cada tubo 2 ml de los pigmentos a analizar.
7) En uno de los tubos de cada pigmento, verter gota a gota la disolución tampón de pH 4, hasta observar color.
8) Introducir el mismo número de gotas de las otras disoluciones tampón y el agua en el resto de los tubos del mismo pigmento.
9) Anotar los cambios observados.
10) Colocar los tubos en un baño se agua hirviendo durante unos 5 minutos.
11) Anotar de nuevo los cambios.

BIBLIOGRAFÍA
o Manual de Química y Bioquímica de los Alimentos. T.P. Coultate. Editorial Acribia S.A. 2ª Edición. 1998.
o http://www.monografias.com/trabajos13/cloro/cloro.shtml
o http://www.food-info.net/es/caro/stru.htm
o http://www.ghmgroup.com/interior.php?IDN=9
o http://otda.state.ny.us/main/language/spanish/FSNEP/2006-09-Shop-SP.pdf
o http://www.saludymedicinas.com.mx/nota.asp?id=2046
o http://www.adaptogeno.com/svms/noticias/noticia311.asp
o http://catarina.udlap.mx/u_dl_a/tales/documentos/lia/acevedo_c_ar/capitulo4.pdf


No hay comentarios:
Publicar un comentario